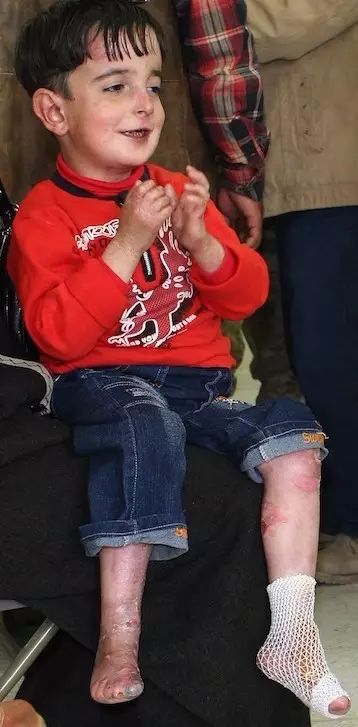
►EB(Epidermolysis Bullosa, 遗传性大疱性表皮松解症)患者的照片。来源:维基百科
编者按:
他们有个美丽的名字:“蝴蝶宝贝”,但美丽的背后是常人难以想像的病痛,因为他们所患的是人类罕见病中公认最痛苦的疾病之一:遗传性大疱性表皮松解症,皮肤像蝴蝶翅膀一样脆弱,而且目前没有安全有效的根治方法。
清华大学药学院和医学院传染病中心谭旭课题组与北京大学第一医院杨勇、林志淼课题组合作发现的是该疾病的第十九个致病基因KLHL24,该研究成果“Stabilizing mutations of KLHL24 ubiquitin ligase cause loss of keratin 14 and human skin fragility”于11月1日以长文形式在线发表于国际遗传学顶尖杂志《自然·遗传学》(Nature Genetics)上,由此或将开启治疗这种罕见病的新希望。
撰文 | 程莉
责编 | 李晓明
● ● ●
遗传性大疱性表皮松解症(Epidermolysis Bullosa, EB)是主要由于皮肤结构蛋白缺陷而导致的一组疾病,患上此病的人皮肤脆性增加,轻微碰撞、摩擦,皮肤上就会出现水疱、糜烂,继发感染,且容易引发严重并发症,如食道粘膜狭窄、手指并指挛缩、角膜瘢痕化导致眼睛失明等。
不同基因突变导致的EB在临床表现上有一定区别,最严重的EB患者出生不久就会因为大片皮肤缺失而早夭,然而较轻型的患者则只在手脚等摩擦频繁的部位出现水疱。
1990年代初,科学家发现第一个导致该病的基因,迄今已有十八个致病基因陆续被发现。任何一个致病基因发生缺陷,都会导致一种亚型的EB。清华大学药学院和医学院传染病中心谭旭课题组与北京大学第一医院杨勇、林志淼课题组合作发现的,是该疾病的第十九个致病基因KLHL24,或者可以说是第十九种EB亚型。
人的皮肤并不是一颗颗细胞简单堆积叠加在一起的,而是由很多结构蛋白像钢筋筑成大楼一样,把细胞和细胞,以及细胞与真皮基质连接起来。以前发现的绝大多数EB患者都是结构蛋白基因发生了突变,皮肤细胞不能正常产生足量的结构蛋白,或者产生了功能缺陷的结构蛋白,因此当皮肤受到机械外力作用,皮肤细胞便会分离或者碎裂——就像一栋钢架质量不好的大楼,抵抗外力强度明显降低,遇到大风或者低强度地震便容易坍塌。
作为国内最大的EB诊疗中心,北京大学第一医院皮肤科常规进行大量EB患者的基因分型和产前诊断工作。在帮助全国各地EB患者的同时,EB工作主要负责人林志淼医生发现有几例EB患者并没有任何已知基因的突变。这使他意识到,他们所患的EB很可能是一种以往从未发现的特殊亚型。这些EB患者出生时即出现大片的皮肤缺失、糜烂,病情较为严重,但随着年龄增长,特别是到青春期或接近成年以后,皮肤脆性会明显自行好转,仅在剧烈的摩擦或活动之后才会起水疱,而且多数不出现严重的并发症。
2014年初,杨勇、林志淼课题组把被疑诊为全新EB亚型的患者进行了全基因组外显子测序,发现其中三个病人都在KLHL24这个基因的起始密码子ATG有一个核苷酸发生了突变。之后,课题组联系了以色列的著名皮肤科专家Eli Sprecher,他提供了一个同样在已知基因中没有找到突变位点的病人,通过基因测序,发现该病人的KLHL24基因的起始密码子也发生了突变。再加上几个月后发现的一个新病人,5位EB病人都是泛素化连接酶编码基因KLHL24的起始密码子发生了突变。
对于这样的发现,课题组一度困惑不已。杨勇回忆说:“我们组做了20年的遗传,这样的事情真是活久见了。起始密码是蛋白质翻译的起点,为什么我们费尽洪荒之力找到的5个病人都在这个位置出现突变呢?突变会造成什么后果,进而导致病人皮肤脆性增加呢?”
杨勇在耶鲁大学进修的时候有个好哥们叫Tony,误以为皮肤科大夫的工作就是“割包皮的”。当杨勇问他为什么对割包皮如此神往,Tony很干脆地回答:New start, more stable!
正是这句话,数年后送来了“神助攻”,让困惑中的团队爆发了灵感:“是否突变会让蛋白质从一个新起点(new start)来翻译,进而蛋白更稳定(more stable)了呢?以往有关这个蛋白的研究极少,在Pubmed文献数据库也只能查到寥寥几篇文章,有限的证据提示它是个泛素化连接酶,能够介导特定底物的降解。是否是这个蛋白变得更稳定以后,加速降解了重要的皮肤结构蛋白,引起皮肤变脆了呢?”
为了验证这个假说,通过北大—清华生命科学联合中心这个平台,杨勇找到了在泛素化领域有很好研究基础的谭旭,经过一系列分子水平的生物化学实验研究,五个特殊病人患病的真相得以揭开。
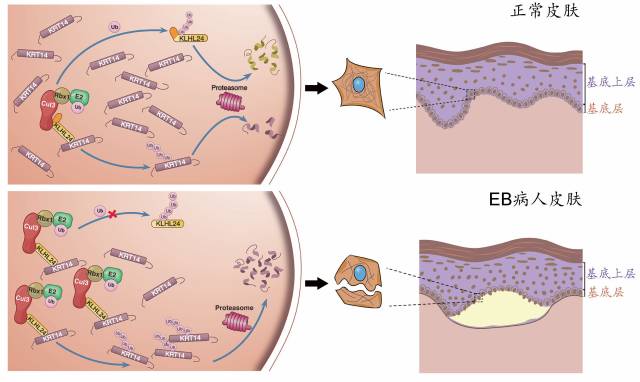
►KLHL24突变所致EB的发病机理示意图:在正常皮肤中(上图),泛素裂解酶KLHL24会发生自身泛素化和降解,因此蛋白维持在较低水平。在EB病人皮肤中KLHL24蛋白的前28个氨基酸缺失,导致其自身泛素化反应和降解被抑制,其蛋白水平大大提高,进一步导致角蛋白14(KRT14) 的过度泛素化和降解,从而使表皮基底层细胞变的脆弱和易脱落。来源:汪慧君供图
皮肤脆性增加,最终还是归结于结构蛋白有缺陷。本次发现的特殊之处在于KLHL24基因并不是控制生产结构蛋白的基因,导致EB的是一种全新的发病机制。
在蛋白翻译的过程中需要有一个ATG负责发出信号告诉蛋白编码机器:“你要在这个特定位置开始翻译出第一个氨基酸来。”这个起始点的密码子ATG就叫起始密码子。当KLHL24的起始密码子发生突变时,便不再能发出信号让蛋白编码机器开始“生产”氨基酸,那么蛋白质按顺序从下一个ATG(第29个密码子)开始翻译,从而丢失前28个氨基酸,生成一种新的截短蛋白。
谭旭课题组主要研究蛋白降解、泛素化以及其在病毒感染疾病中的功能,他们在这项研究中发现,突变后KLHL24截短蛋白因自身泛素化及随之蛋白降解受到抑制而变得稳定许多,从而导致细胞中的KLHL24蛋白量增加。进一步的研究发现皮肤的角蛋白14是KLHL24的一个蛋白底物,过量的KLHL24导致其角蛋白14发生过度泛素化和降解。这些在细胞系上发现的现象在病人皮肤样品上得到了验证,与正常人相比,病人的角蛋白14的水平大大降低,直接导致皮肤脆性增强。谭旭把这个泛素连接酶的自身泛素化和降解过程称为“一个连环杀手的自杀事件”。
简单来说,这类EB患者本身生产的结构蛋白是没有问题的,但是有一个工作积极性过高的“杀手”把他们都“杀死”了。这个“杀手”就是泛素化连接酶编码基因KLHL24突变后产生的截短蛋白,这个“谋杀”的过程叫泛素化(ubiquitination)。泛素化连接酶的重要作用是识别降解我们人体的一些需要精密调控的蛋白或者不需要的蛋白,但是为保持平衡,同时它也可以把自己降解掉,是为自身泛素化(autoubiquitination), 类似“自杀”。KLHL24突变后,其自身泛素化水平下降,它们变得更稳定,不“自杀”了。后果是这种“杀手”数量过多,进而导致大量正常的皮肤角蛋白14被泛素化及降解。
角蛋白14存在于我们皮肤表皮最底层的细胞间,是皮肤基底细胞形成张力丝的关键蛋白,和真皮胶原蛋白连接在一起,维持表皮细胞结构稳定。如果角蛋白14被过度降解,表皮跟真皮的连接会变脆弱,皮肤脆性增加,也就是EB的临床表现。林志淼介绍说,有一种类型的EB,叫基底细胞型单纯型EB,就是由于角蛋白14缺陷所致的。
研究同时发现,KLHL24是一种调节正常表皮细胞分化的重要基因。在此之前,由于小鼠模型难以建立,也没有对角蛋白的分子水平的研究,人们并不知道连接酶与蛋白降解之间存在什么关系,更不清楚如何调节角蛋白降解。此次研究揭示的这种全新的机制,更大的意义在于对调节其它蛋白特别是其它角蛋白降解的启示。
如何运用药物分子调控这个过度活跃的“杀手”,让它恢复正常功能水平,是两个课题组接下来继续研究的方向。“我们正在研发一种多肽抑制剂,这种新型的抑制剂将来也许能够实现治疗此种亚型的EB。”谭旭透露说。
与EB致病基因相反,有些基因突变后,角蛋白过度产生,异常角蛋白会干扰正常角蛋白发挥功能。将来也许可以通过激活蛋白泛素化和降解系统,用来降解、泛素化异常结构的角蛋白,让正常的角蛋白发挥功能,从而治疗一些角蛋白缺陷的疾病。“比如有些人经过轻微摩擦便会出现又厚又硬的茧子,还有些人头发像羊毛一样细软,这些都是是皮肤科常见的角蛋白缺陷造成的疾病。” 林志淼说。
在临床实践中,遗传病从发现基因、了解发病原理到能够出现有效的治疗办法,过程很缓慢,甚至需要多方科研工作者几十年的奋斗。EB作为一种罕见病,所有的类型都算上,据林志淼估计,全国约有上万病例,其中重型的有几千例,轻型的较多而且会遗传。正因为是罕见病,市场需求有限,药商往往不感兴趣,不愿意生产。这是罕见病治疗中存在的一个大问题。
对EB的治疗,目前除了骨髓移植,没有更好的治疗办法。即使骨髓移植有20%~30%的死亡率,且有1/3的几率效果不明显,特别严重的EB患者,还是甘冒风险。迄今中国只有两例骨髓移植成功的病人,其中一例是营养不良型大疱性表皮松解症患者周密。因为女儿的病,周密的父亲周迎春创建了公益组织“上海德博蝴蝶宝贝关爱中心”并担任理事长,长期关注EB的宣传教育、关怀救助等工作。病人和家属都急切盼望医学研究者能多关注这个疾病,早日开发出更有效的治疗方法。
北京大学第一医院是EB的诊治中心,面对从全国各地赶来诊断和初步治疗护理的患者,作为临床医生,林志淼最关心的是如何减轻他们的痛苦。“EB治疗中最重要的是避免摩擦、护理伤口,防治并发症。” 林志淼说,“如果病人不好好护理的话会产生各种不良后果。”尤其是手、脚容易摩擦的地方最易起水疱,如果在护理过程中,没有把指头分开包扎,手指并在一起,由于皮肤修复过程中会倾向于最短途径,损伤破口的相邻手指会长在一起。在睡觉时,人类的手指处于自然弯曲状态,如不经干涉,手指便会蜷缩在一起,影响患儿骨骼发育,造成完全残疾。
大疱性表皮松解症患者忍受着常人难以想象的痛苦,杨勇说:“作为临床医生,我们有责任为疾病的研究和治疗付出最大的努力。没有林志淼辛勤的临床工作和扎实的遗传功底,就没有今天的故事;谭旭严谨详实的工作揭开了角蛋白泛素化的神秘面纱;清华的李硕和北大的冯程通力合作,完成了大部分的实验操作;以色列的Eli Sprecher、清华的邓海腾,北京生命科学研究所的陈婷也做了重要贡献,还要感谢众多的合作者。最后,我还想感谢Tony,呃,和他的‘新起点’。”
论文链接:http://dx.doi.org/10.1038/ng.3701